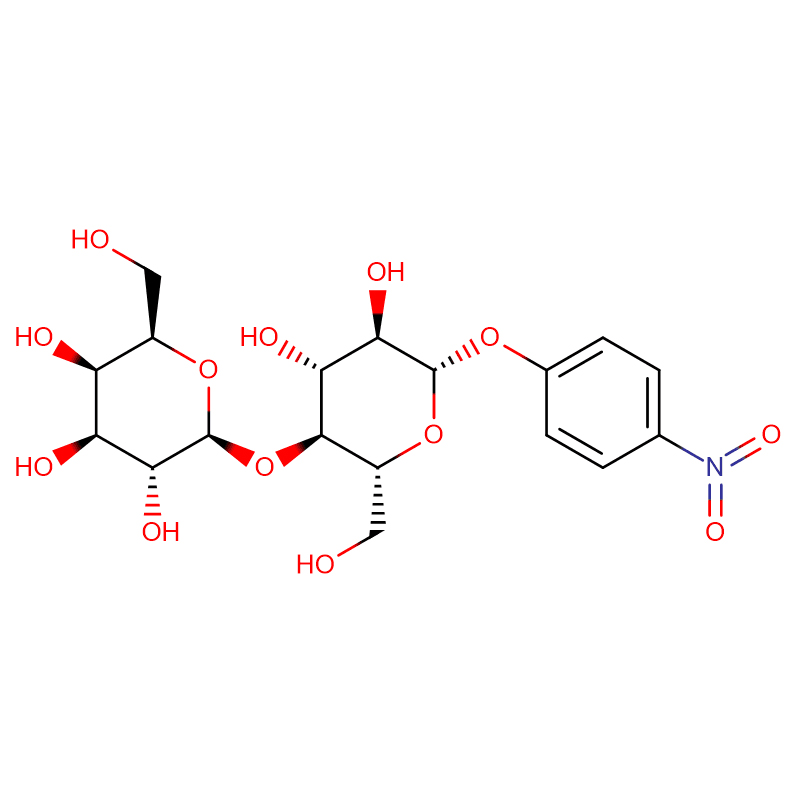
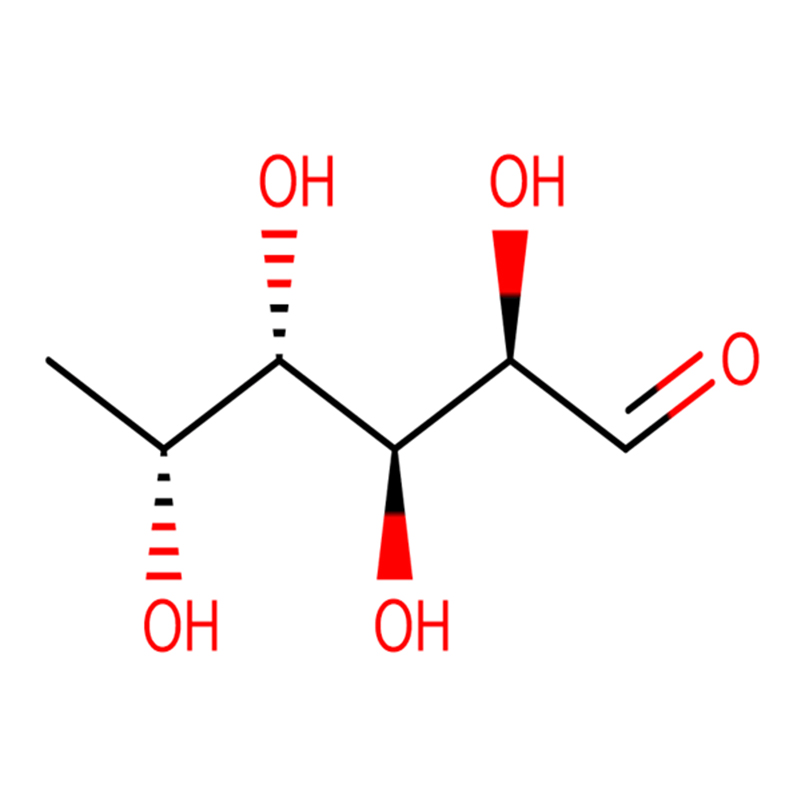
دو آنالوگ ایزومری بی سیکلو[4.1.0] هپتان از بازدارنده گلیکوزیداز گالاکتووالیدامین، (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(هیدروکسی متیل)بی سیکلو[4.1.0]هپتان -2،3،4-triol، در 13 مرحله از 2،3،4،6-tetra-O-benzyl-D-گالاکتوز سنتز شده است.فعالیت های مهاری دو آمین محدود شده از نظر ساختاری، و استامیدهای مربوطه آنها، در برابر آنزیم های تجاری آلفا-گالاکتوزیداز از دانه قهوه و E. coli اندازه گیری شد.فعالیت آنزیم GH27 خانواده گلیکوزیل هیدرولاز (دانه قهوه) به طور رقابتی توسط 1R,6S-آمین (7) مهار شد، یک تعامل اتصال که با مقدار K(i) 0.541 میکرومولار مشخص شد.GH36 E. coli آلفا-گالاکتوزیداز تعامل اتصال بسیار ضعیف تری با 1R،6S-آمین (IC(50) = 80 میکرومولار) از خود نشان داد.دیاسترئومر 1S،6R-آمین (9) ضعیف به هر دو گالاکتوزیداز، (دانه قهوه، IC(50) = 286 میکرومولار) و (E. coli، IC(50) = 2.46 میلی مولار) متصل می شود.